今天我们来聊一聊MDD及MDR下的技术文件
MDR下的技术文件简要
证明该器械符合医疗器械指令/法规的规定,尤其是与指令/法规要求的符合性。
产品的制造必须与技术文件描述的相一致。
公告机构和监管机构基于技术文件对产品的符合性进行评价。
技术文件至少向主管机构开放10年,若为可植入器械,周期应至少为最后器械投放市场后的15年。经主管机构要求,制造商应能提供完整的技术文件。
欧盟授权代表也应保留一份可用的技术文件。
MDD/MDR技术文件的要求
技术文件应包含的内容在医疗器械相关的指令/法规中都进行了要求:
MDD:
医疗器械指令MDD 93/42/EEC:附录II到VII
公告机构协会NB-MED2.5.1 rec5 rev4 技术文件指南 (PartA & PartB)
MDR:
医疗器械法规MDR (EU)2017/745: 附录II技术文件,附录III上市后监督技术文件
MDD附录技术文件内容
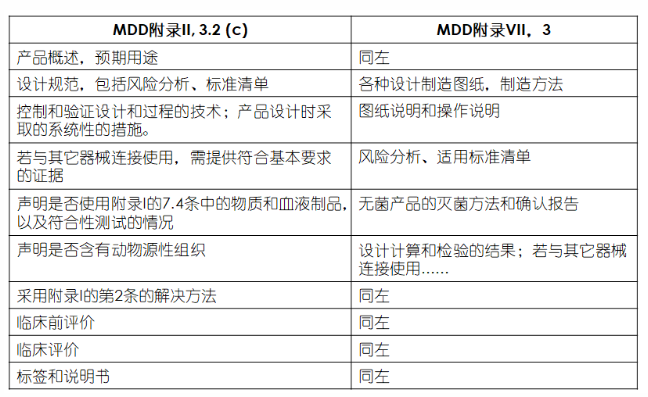
MDR附录技术文件内容